MARTES
¿Qué grupos funcionales están presentes en los nutrimentos orgánicos?
Equipo | Familia | Nombre Grupo funcional | ejemplos | usos | |
1 | Alcanos Alquenos | Eteno: CH 2 = CH 2 CH3CH2Br + KOH → CH2=CH2 + H2O + KBr | . La elevada reactividad del doble enlace los hace importantes intermediarios de la síntesis de una gran variedad de compuestos orgánicos. Probablemente el alqueno de mayor uso industrial sea el ETILENO (eteno) que se utiliza entre otras cosas para obtener el plástico POLIETILENO, de gran uso en cañerías, envases, bolsas y aislantes eléctricos. También se utiliza para obtener alcohol etílico, etilen-glicol, cloruro de vinilo y estireno | ||
2 | Alquinos Alcoholes | . | |||
3 | Ácidos Cetonas | . | |||
4 | Aldehidos Aminas | CH3-NH2 Metilamina o aminometano CH3-NH-CH3 Dimetilamina o metilaminometano | Las aminas alifáticas se emplean en las industrias química, farma- céutica, de caucho, plásticos, colorantes, tejidos, cosméticos y metales. Sirven como productos químicos intermedios, disolventes, aceleradores del caucho, catalizadores, emulsionantes, lubricantes sintéticos para cuchillas, inhibidores de la corrosión y agentes de flotación. Muchas de ellas se emplean en la fabricación de herbicidas, pesticidas y colorantes. En la industria foto- gráfica, la trietilamina y la metilamina se utilizan como aceleradores para reveladores. La dietilamina se utiliza como inhibidor de la corrosión en las industrias metalúrgicas y como disolvente en la industria del petróleo. En las industrias de curtidos y cuero, la hexametilentetramina se utiliza como conservante de curtidos; la meti- lamina, la etanolamina y la diisopropanolamina son agentes reblandecedores de pieles y cuero. | ||
5 | Amidas Esteres | RCONR'R | La acrilamida.-se emplea en distintas aplicaciones, aunque es más conocida por ser probablemente carcinógena y estar presente en bastantes alimentos al formarse por procesos naturales al cocinarlos. son fuente de energia para el cuerpo humano. Por ejemplos pueden ser vitaminas en el cuerpo o analgésicos. Las grasas, que son ésteres de glicerina y ácidos grasos (ácido oleico, ácido esteárico, etc.) | Las amidas son comunes en la naturaleza y se encuentran en sustancias como los aminoácidos, las proteínas, el ADN y el ARN, hormonas, vitaminas. Es utilizada en el cuerpo para la excreción del amoníaco ( NH3) Muy utilizada en la industria farmacéutica, y en la industria del nailon. Los esteres pueden participar en los enlaces de hidrógeno como aceptadores, pero no pueden participar como dadores en este tipo de enlaces, a diferencia de los alcoholes de los que derivan | |
6 | Cíclicos Policiclicos |   | Cíclicos: Ciclobutano 1-etil-3-metil-5-propil-ciclohexano 3,4,5-trimetil-ciclohexeno Policiclicos: Antraceno An Fenantreno Ph Fluoranteno Fl Pireno Py Criseno Chry Naftaleno Np | Hidrocarburos cíclicos: Son cadenas cerradas que se dividen en Aliciclicos (cicloalcanos, cicloalquenos y cicloaquinos) y Aromáticos (anillos aromaticos e insaturados). Existen compuestos que tienen varios anillos unidos, los policíclicos. Cicloalcanos: ciclo formado por enlaces simples. El más simple de todos es el ciclopropano. Cicloalquenos: Hidrocarburos cíclicos con enlaces doble. El más simple es el ciclopropeno Cicloalquinos: presentan triples enlaces. El más simple es el ciclopropino. Casi todo el antraceno es oxidado para dar antraquinona y por lo tanto sustancia de partida en la síntesis de una amplia gama de colorantes como la alizarina. Además se utiliza en la síntesis de algunos insecticidas, conservantes, etc. |
Sustancias en los alimentos
Material: tintura de yodo , almidón, sal refinada  , sal de grano,
, sal de grano,
papas , bolillo o pan de caja
, bolillo o pan de caja  , tortilla de harina
, tortilla de harina  , pastillas de vitamina C(acido ascórbico)
, pastillas de vitamina C(acido ascórbico)  , semillas de trigo,
, semillas de trigo,  agua, , gotero
agua, , gotero  , capsula de porcelana, navaja, limones(acido cítrico)
, capsula de porcelana, navaja, limones(acido cítrico)  y una bebida de fruta.
y una bebida de fruta. 
papas


a) Preparación de reactivos
- Colocar unas gotas de la solución de yodo en un vaso y agregar agua para lograr una solución diluida que debe quedar de un color amarillo claro.
- Poner una pequeña cantidad de almidón en un vaso y añadir un poco de agua y agitar, resulta una suspensión blanquisca.
- Poner una pequeña cantidad de almidón en un vaso y añadir un poco de agua y agitar, resulta una suspensión blanquisca.
b) Determinación de almidón
- Cortar con mucho cuidado, ayudado con un navaja los extremos a 4 semillas de trigo. O el pan.
- Colocar por separado en la capsula de porcelana: una pequeña cantidad de la suspensión de almidón, unas tiras de la tortilla de harina, un fragmento de migajón de pan, unas tiras de la tortilla de maíz y 3 semillas de trigo sin los extremos.
- Añadir a cada sustancia unas 5 gotas de la solución diluida de yodo.
- Observar que acontece:
- Colocar por separado en la capsula de porcelana: una pequeña cantidad de la suspensión de almidón, unas tiras de la tortilla de harina, un fragmento de migajón de pan, unas tiras de la tortilla de maíz y 3 semillas de trigo sin los extremos.
- Añadir a cada sustancia unas 5 gotas de la solución diluida de yodo.
- Observar que acontece:
c) Determinación de yodo
- Moler unos cuantos granos de sal en grano hasta que quede un polvo fino
- Colocar por separado en 2 tapas de refresco(capsula e porcelana) sal en grano molida y sal de mesa
- Añadir a ambas tapas una pequeña cantidad de almidón en polvo
- Agregar a las dos tapas un poco de agua
-Esperar 10 minutos y observar
- Colocar por separado en 2 tapas de refresco(capsula e porcelana) sal en grano molida y sal de mesa
- Añadir a ambas tapas una pequeña cantidad de almidón en polvo
- Agregar a las dos tapas un poco de agua
-Esperar 10 minutos y observar
d) Determinación de vitamina C
- Moler la pastilla de vitamina C (Acido ascórbico)
- Exprimir un limón y obtener un poco de jugo
- Colocar en una capsula de porcelana un poco de polvo de vitamina C(acido as orbico), añadir agua y disolver.
- En la capsula poner por separado, jugo de limón(acdio cítrico) y una bebida de frutas
- Añadir a todas las tapas 3 gotas de solución diluida de yodo y agitar
- Finalmente colocar en cada tapa 5 gotas de la suspensión de almidón, esperar 2 minutos y observar
- Exprimir un limón y obtener un poco de jugo
- Colocar en una capsula de porcelana un poco de polvo de vitamina C(acido as orbico), añadir agua y disolver.
- En la capsula poner por separado, jugo de limón(acdio cítrico) y una bebida de frutas
- Añadir a todas las tapas 3 gotas de solución diluida de yodo y agitar
- Finalmente colocar en cada tapa 5 gotas de la suspensión de almidón, esperar 2 minutos y observar
Observaciones:
Actividad | Observaciones: |
A | |
B | cambia de color |
C | el pan no se limpia totalmente |
D | la papa se limpia |
Conclusiones: La mayoría de los alimentos contiene almidón, que este a su vez se convierte en carbohidratos. Esta es una molécula muy grande que contiene polímeros que se endurece cuando le das energía calorífica para hacer la polimerización.
JUEVES
ANALISIS DE UN “GANSITO”
CONSEGUIR UN GANSITO PARA ANALIZAR LOS COMPUESTOS QUE LO FORMAN:
| NOMBRE DEL COMPUESTO | FORMULA CONDENSADA | ESTRUCTURA | ORIGEN | USOS |
| colesterol | C27H46O | | se encuentra en los tejidos corporales y en el plasma sanguíneovertebrados. de los | éste ayuda a que las actividades orgánicas se realicen satisfactoriamente. |
| Fibra dietética | | | se puede definir como la parte de las plantas comestibles que resiste la digestión y absorción en el intestino delgado humano y que experimenta una fermentación parcial o total en el intestino grueso. Esta parte vegetal está formada por un conjunto de compuestos químicos de naturaleza heterogénea | la fibra alimentaria desempeña funciones fisiológicas sumamente importantes como estimular la peristalsis intestinal |
| Grasa mono insaturada | C18H34O2 | | es un término genérico para designar varias clases de lípidos, aunque generalmente se refiere a los acilglicéridos, ésteres en los que uno, dos o tres ácidos grasos se unen a una molécula de glicerina, formando monoglicéridos, diglicéridos y triglicéridos respectivamente. | Las grasas o lípidos y los hidratos de carbono, son las principales fuentes de energía. |
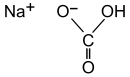
| Bicarbonato de sodio | NaHCO3 | | Se puede encontrar como mineral en la naturaleza o se puede producir artificialmente | se utiliza como un agente alcalinizante que actua en combinación a la saliva en el coqueo, de manera que se suaviza y se produce la extraccion de los metabolitos de la hoja de coca haciéndose de esa manera el coqueo un proceso placentero y duradero en contraposicion si no se usara el bicarbonato de sodio. |
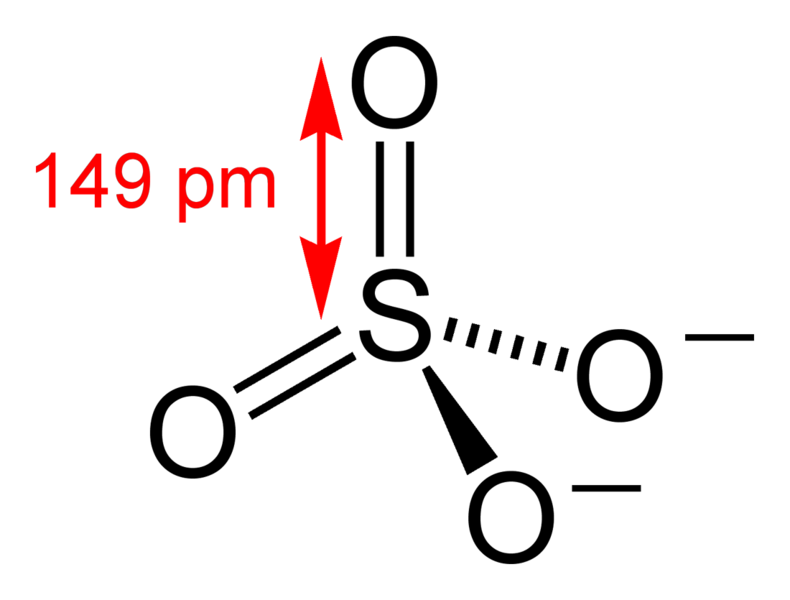
| Sulfato | SO4 | | Los sulfatos inorgánicos son las sales del ácido sulfúrico. | Las aplicaciones de los sulfatos suelen variar enormemente según el metal al que están unidos. Así el sulfato sódico, por ejemplo, se utiliza en la fabricación del vidrio, como aditivo en los detergentes, etc.; el sulfato de cobre se aprovecha en la fabricación de la viscosa según un determinado proceso. |
| Fosfato de aluminio | Al(PO4) | | Es el tercer elemento más común encontrado en la corteza terrestre. Los compuestos de aluminio forman el 8% de la corteza de la tierra y se encuentran presentes en la mayoría de las rocas, de la vegetación y de los animales.[ | posee una combinación de propiedades que lo hacen muy útil en ingeniería mecánica, tales como su baja densidad3) y su alta resistencia a la corrosión. Mediante aleacionesresistencia mecánica (hasta los 690 MPa). Es buen conductor de la electricidad y del calor, se mecaniza con facilidad y es relativamente barato. (2.700 kg/m adecuadas se puede aumentar sensiblemente su |
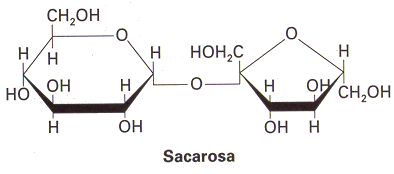
| Almidón | (C6H10O5)n | | es un polisacáridoplantas, constituido por amilosa y amilopectina. de reserva alimenticia predominante en las | ienen un número enorme de posibles aplicaciones en los alimentos, que incluyen las siguientes: adhesivo, ligante, enturbiante, formador de películas, estabilizante de espumas, agente anti-envejecimiento de pan, gelificante, glaseante, humectante, estabilizante, texturizante y espesante. |
| Glucosa | C6H12O6 | | es un monosacárido con fórmula molecularC6H12O6, la misma que la fructosa pero con diferente posición relativa de los grupos -OH y O=. | es de mucho uso en la repostería, para la elaboración de Masa Elástica, Fondant, relleno para bombones, relleno para chocotejas, en la elaboración de caramelo y golosinas. |
| Azucares | C12H22O11 | | es un disacáridoglucosa y una de fructosa, que se obtiene principalmente de la caña de azúcarremolacha. formado por una molécula de o de la | la función del azúcar en nuestro organismo es proporcionar la energía que se necesita para el funcionamiento de los diferentes órganos, También * Como endulzante de refrescos, zumos, tes, infusiones, chocolate, mermeladas, galletas. |
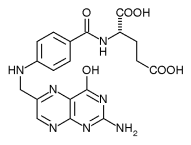
| Acido fólico | C19H19N7O6 | | es una vitaminahidrosolubleproteínashemoglobina (y por esto, transitivamente, de los glóbulos rojos); su insuficiencia en los humanos es muy rara. Es una vitamina del complejo de vitaminas B que se encuentra en algunos alimentos enriquecidos y en forma sintética (es decir, más fácil de asimilar). necesaria para la formación de estructurales y | |
| Calcio | Ca | | Se encuentra en el medio interno de los organismos como ion calcio (Ca2+) o formando parte de otras moléculas; en algunos seres vivos se halla precipitado en forma de esqueleto interno o externo. | Desoxidante, desulfurizador, o decarburizador para varias aleaciones ferrosas y no ferrosas. Aplicación en muchos productos lácteos o medicamentos para el refuerzo de los huesos humanos, compuestos de calcio. Si tenemos falta de calcio en nuestros huesos facilitaremos la aparición de enfermedades como la osteoporosis. |
| Grasas saturadas | C18H34O2 | | es un término genérico para designar varias clases de lípidos, aunque generalmente se refiere a los acilglicéridos, ésteres en los que uno, dos o tres ácidos grasos se unen a una molécula de glicerina, formando monoglicéridos, diglicéridos y triglicéridos respectivamente. | Las grasas o lípidos y los hidratos de carbono, son las principales fuentes de energía. |
| Yodo | I | | Este elemento puede encontrarse en forma molecular como yodo diatómico. | Es un oligoelemento y se emplea principalmente en medicina, fotografíacolorante. Químicamente, el yodo es el halógeno menos reactivo y electronegativo. y como |
| Zinc | Zn | | El zinc es un metal, a veces clasificado como metal de transición aunque estrictamente no lo sea, ya que tanto el metal como su especie dispositiva presentan el conjunto orbital completo | Otros usos incluyenBaterías de Zn-AgO usadas en la industria aeroespacial para misiles y cápsulas espaciales por su óptimo rendimiento por unidad de peso y baterías zinc-aire para computadoras portátiles. Piezas de fundición inyectada en la industria de automoción. Metalurgia de metales preciosos y eliminación de la plata del plomo. |
| Hierro | Fe | | Este metal de transición es el cuarto elemento más abundante en la corteza terrestre, representando un 5% y, entre los metales, sólo el aluminio es más abundante. | El acero es indispensable debido a su bajo precio y tenacidad, especialmente en automóviles, barcos y componentes estructurales de edificios. Las aleaciones férreas presentan una gran variedad de propiedades mecánicas dependiendo de su composición o el tratamiento que se haya llevado a cabo. |
| Huevo | | | Los más consumidos, con gran diferencia, son los de gallinaGallus gallus), seguidos por los de pato y oca, también se consumen los huevos de codorniz que son muy pequeños, bien como exquisitez gastronómica o para niños pequeños. ( | |
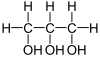
| Glicerina | C3H8O3 | | El 1,2,3 propanotriol, glicerol o glicerina(C3H8O3) (del griego Glykos, dulce) es un alcohol con tres grupos hidroxilos (–OH), por lo que podemos representar la molécula como o, en su forma semidesarrollada como,  . El propanotriol es uno de los principales productos de la degradación digestiva de los lípidos, paso previo para el ciclo de Krebs y también aparece como un producto intermedio de la fermentación alcohólica . El propanotriol es uno de los principales productos de la degradación digestiva de los lípidos, paso previo para el ciclo de Krebs y también aparece como un producto intermedio de la fermentación alcohólica |
|
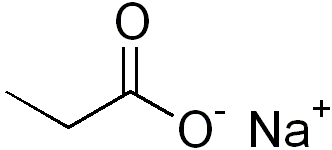
| Propinato de sodio | Na(C2H5COO). | | es la sal sódicaácido propanoico con la fórmula químicaNa(C2H5COO). del | También se utiliza para prevenir la cetosis en los bovinos durante el periodo periparto. |
| Carboximetilcelulosa | C6H7O2 OH | | a la inversa de los demás estabilizantes vegetales, son mucho menos solubles en caliente que en frío. La viscosidad depende mucho del grado de substitución. | Actúan fundamentalmente como agentes dispersantes, para conferir volumen al alimento y para retener la humedad. |
| Soya | | | Aunque con un notable diferencial inferior en su precio, la cotización internacional de la soja es paralela a la de la harina de pescado. Cuando escasea la soja, sube automáticamente el precio de la harina de pescado y viceversa. El gran valor proteínico de la legumbre (posee los ocho aminoácidos esenciales) lo hace un gran sustituto de la carne en culturas veganas. De la soja se extraen subproductos como la leche de soja o la carne de soja. | |
| Sorbitol | C6H14O6 | | En la naturaleza el sorbitol es uno de los tres glucidos (sacarosa, almidón y sorbitol) principales producidos por la fotosíntesis en las hojas adultas de ciertas plantas de las familias Rosaceae y Plantaginaceae. | Es un sólido higroscópico que se utiliza en la industria como humectante para mantener diversos productos con un grado de humedad apropiado, se utiliza en la elaboración de alimentos, fármacos y productos químicos. Acondicionador de papel, textiles, colas y cosméticos, también como emulsionante en la fabricación de pasteles y dulces para impedir que se separen la fase acuosa y la fase grasa en estos alimentos; el sabor dulce relativo de la sacarosa-sorbitol es de 100-60 por lo tanto necesitaremos una cantidad mayor de sorbitol para obtener el mismo sabor dulce que el azúcar de mesa. Además, el sorbitol se utiliza como fuente de alcohol en la fabricación de resinas. |
| Cocoa | | | A partir de esta combinación básica, se elaboran los distintos tipos de chocolate, que dependen de la proporción entre estos elementos y de su mezcla o no con otros productos tales como leche y frutos secos. | |
| Monogliceridos de acidos grasosos | CH3–(CH2)n–COOH. | | es una biomoléculaorgánica de naturaleza lipídicahidrocarbonada lineal, de número par de átomos de carbono, en cuyo extremo hay un grupo carboxilo. formada por una larga cadena | |
| Acido benzoico | C6H5-COOH | | es un ácido carboxílico aromático que tiene un grupo carboxilo unido a un anillo fenílico. En condiciones normales se trata de un sólido incoloro con un ligero olor característico. Es poco soluble en agua fría pero tiene buena solubilidad en agua caliente o disolventes orgánicos. | El ácido benzoico y sus derivados sólo se pueden utilizar para conservar alimentos con un pH ácido. Protege sobre todo contra el moho (también las variantes que producen las aflatoxinas) y fermentaciones no deseadas, a veces se utiliza conjuntamente con el dióxido de azufre2) o los sulfitos (SO para atacar un espectro más amplio de microorganismos. También es producto de partida en la producción de ésteres del ácido benzoico que se utilizan en perfumería. |
| Esteres de poliglicerol | | | Los poligliceril ésteres son sustancias que se obtienen por esterificación de poliglicerol con ácidos carboxílicos de cadena saturada. El poliglicerol es el resultado de la polimerización en medio básico de la glicerina, mediante reacciones de deshidratación, dando lugar a enlaces éter entre las distintas unidades. | Su principal aplicación es como emulsificantes w/o y o/w. Incluso los compuestos más hidrófobos de este grupo, como el poligliceril-10 decaoleato, pueden dar lugar a emulsiones estables del tipo agua en aceite. |
| Polisorbato Saborizante arfiticial | | | Los Saborizantes son preparados de sustancias que contienen los principios sápido-aromáticos, extraídos de la naturaleza(vegetal) o sustancias artificiales, de uso permitido en términos legales, capaces de actuar sobre los sentidos del gusto y del olfato, pero no exclusivamente, ya sea para reforzar el propio (inherente del alimento) o transmitiéndole un sabor y/o aroma determinado, con el fin de hacerlo más apetitoso pero no necesariamente con este fin. | Es de uso habitual la utilización de las palabras sabores, esencias, extractos y oleorresinas como equivalentes a los saborizantes. |
| Azúcar | C12H22O11 | | se obtiene principalmente de la caña de azúcarremolacha. o de la | la función del azúcar en nuestro organismo es proporcionar la energía que se necesita para el funcionamiento de los diferentes órganos, También * Como endulzante de refrescos, zumos, tes, infusiones, chocolate, mermeladas, galletas. |
| Leche reconstituida | C12H22O11·H2O | | es una secreción nutritiva de color blanquecino opaco producida por las glándulas mamarias de las hembras | s muy frecuente el empleo de los derivados de la leche en las industrias agroalimentarias, químicas y farmacéuticas en productos como la leche condensada, leche en polvo, caseína o lactosa. |
| Harina de trigo | | | cultivados como silvestres, que pertenecen al género Triticum; son plantas anuales de la familia de las gramíneas, ampliamente cultivadas en todo el mundo | es utilizado para hacer harina, harina integral, sémola, cerveza y una gran variedad de productos alimenticios. |
| Goma arabica | | Hoy en día la mayor parte se utiliza en la industria alimentaria para fijar aromas, estabilizar espumas y emulsiones, modificar la consistencia de alimentos o clarificar vinos. También se utiliza en la fabricación de algunos medicamentos. | ||
| Goma xantana | | | producido por la bacteriaXanthomonas campestris B-1459. | produciendo soluciones de viscosidad relativamente alta a concentraciones bajas |
RECAPITULACIÓN:
El dia martes vimos el tema de ¿Qué grupos funcionales estan presentes en los nutrimentos organicos? donde realizamos un experimento y vimos que reacciones tenía con el almidon.
El día jueves realizamos el analisis de un gansito, pero no terminamos por falta de internet.
INDAGACIONES:
¿Qué grupos funcionales estan presentes en los nutrimentos organicos?
Siendo los compuestos orgánicos, el tipo de sustancias más abundante en la naturaleza a diario se sintetizan miles de nuevos compuestos; sin lugar a dudas los hidrocarburos son los compuestos orgánicos más simples en su composición, ya que únicamente están formados por carbono e hidrógeno.
Al átomo o grupo de átomos que representa la diferencia entre un
Hidrocarburo y el nuevo compuesto se le denomina grupo funcional.
Es decir que un grupo funcional es un átomo o grupo de átomos que identifica
a una clase de compuestos orgánicos.
Cada grupo funcional da lugar a una determinada serie de propiedades
Químicas semejantes para todos los compuestos que los contengan.
Se llama función química a las propiedades comunes que caracterizan a
un conjunto de sustancias que tienen estructura semejante, es decir,
que poseen a un determinado grupo funcional.
un conjunto de sustancias que tienen estructura semejante, es decir,
que poseen a un determinado grupo funcional.
Alcanos:
Los alcanos son hidrocarburos, es decir que tienen sólo átomos de carbono e hidrógeno. La fórmula general para alcanos alifáticos (de cadena lineal) es CnH2n+2, y para cicloalcanos es CnH2n. También reciben el nombre de hidrocarburos saturados.
Los alcanos se presentan en estado gaseoso, líquido o sólido según el tamaño de la cadena de carbonos. Hasta 4 carbonos son gases (metano, etano, propano y butano), a partir del pentano hasta el hexadecano (16 carbonos) son líquidos y los compuestos superiores a 16 carbonos se presentan como sólidos aceitosos (parafinas). Todos los alcanos son combustibles, al ser una forma reducida del carbono, y liberan grandes cantidades de energía durante la combustión.
Los alcanos se presentan en estado gaseoso, líquido o sólido según el tamaño de la cadena de carbonos. Hasta 4 carbonos son gases (metano, etano, propano y butano), a partir del pentano hasta el hexadecano (16 carbonos) son líquidos y los compuestos superiores a 16 carbonos se presentan como sólidos aceitosos (parafinas). Todos los alcanos son combustibles, al ser una forma reducida del carbono, y liberan grandes cantidades de energía durante la combustión.
Alquenos:
Los alquenos son hidrocarburos que tienen doble enlace carbono-carbono en su molécula, y por eso son denominados insaturados. La fórmula genérica es CnH2n. Se puede decir que un alqueno no es más que un alcano que ha perdido un hidrógeno produciendo como resultado un enlace doble entre dos carbonos.
Al igual que ocurre con otros compuestos orgánicos, algunos alquenos se conocen todavía por sus nombres no sistemáticos, en cuyo caso se sustituye la terminación -eno sistemática por -ileno, como es el caso del eteno que en ocasiones se llama etileno, o propeno por propileno. Los alquenos cíclicos reciben el nombre de cicloalquenos.
Al igual que ocurre con otros compuestos orgánicos, algunos alquenos se conocen todavía por sus nombres no sistemáticos, en cuyo caso se sustituye la terminación -eno sistemática por -ileno, como es el caso del eteno que en ocasiones se llama etileno, o propeno por propileno. Los alquenos cíclicos reciben el nombre de cicloalquenos.
Alquinos
Los alquinos son hidrocarburos alifáticos con al menos un triple enlace entre dos átomos de carbono. Se trata de compuestos metaestables debido a la alta energía del triple enlace carbono-carbono. Su fórmula general es CnH2n-2
Los alquinos pueden ser hidrogenados par dar los cis-alquenos correspondientes con hidrógeno en presencia de un catalizador de paladio sobre sulfato de bario o sobre carbonato cálcico parcialmente envenenado con óxido de plomo. Si se utiliza paladio sobre carbón activo el producto obtenido suele ser el alcano correspondiente.
Los alquinos pueden ser hidrogenados par dar los cis-alquenos correspondientes con hidrógeno en presencia de un catalizador de paladio sobre sulfato de bario o sobre carbonato cálcico parcialmente envenenado con óxido de plomo. Si se utiliza paladio sobre carbón activo el producto obtenido suele ser el alcano correspondiente.
Alcoholes:
En química se denomina alcohol (del árabe al-khwl الكحول, o al-ghawl الغول, "el espíritu", "toda sustancia pulverizada", "líquido destilado") a aquellos hidrocarburos saturados, o alcanos que contienen un grupo hidroxilo (-OH) en sustitución de un átomo de hidrógeno enlazado de forma covalente.
Los alcoholes pueden ser primarios, secundarios o terciarios, en función del número de átomos de hidrógeno sustituidos en el átomo de carbono al que se encuentran enlazado el grupo hidroxilo.
A nivel del lenguaje popular se utiliza para indicar comúnmente una bebida alcohólica, que presenta etanol, con formula química CH3CH2OH.
Los alcoholes pueden ser primarios, secundarios o terciarios, en función del número de átomos de hidrógeno sustituidos en el átomo de carbono al que se encuentran enlazado el grupo hidroxilo.
A nivel del lenguaje popular se utiliza para indicar comúnmente una bebida alcohólica, que presenta etanol, con formula química CH3CH2OH.
Cetonas:
es un compuesto orgánico caracterizado por poseer un grupo funcional carbonilo.[1] Cuando el grupo funcional carbonilo es el de mayor relevancia en dicho compuesto orgánico, las cetonas se nombran agregando el sufijo -ona al hidrocarburo del cual provienen (hexano, hexanona; heptano, heptanona; etc). También se puede nombrar posponiendo cetona a los radicales a los cuales está unido (por ejemplo: metilfenil cetona). Cuando el grupo carbonilo no es el grupo prioritario, se utiliza el prefijo oxo- (ejemplo: 2-oxopropanal).
Ácidos:
Un ácido (del latín acidus, que significa agrio) es considerado tradicionalmente como cualquier compuesto químico que, cuando se disuelve en agua, produce una solución con una actividadcatión hidronio mayor que el agua pura, esto es, un pH menor que 7. Esto se aproxima a la definición moderna de Johannes Nicolaus Brønsted y Martin Lowry, quienes definieron independientemente un ácido como un compuesto que dona un catión hidrógeno (H+) a otro compuesto (denominado base). Algunos ejemplos comunes incluyen al ácido acético (en el vinagre), y el ácido sulfúrico (usado en baterías de automóvil). Los sistemas ácido/base son diferentes de las reacciones redox en que no hay un cambio en el estado de oxidación. Los ácidos pueden existir en forma de sólidos, líquidos o gases, dependiendo de la temperatura. También pueden existir como sustancias puras o en solución.
de
de
Amidas:
Una amida es un compuesto orgánico cuyo grupo funcional es de RCONRlRll, siendo CO el grupo funcional carbonilo, N un átomo de nitrógeno, y R, Rl, Rll radicales orgánicos o átomos de hidrógeno.
Se puede considerar como un derivado de un ácido carboxílico por sustitución de grupo oxidrilo (-OH) del ácido por un grupo –NH2, -NHR ó –NRRl llamado grupo amino.
En síntesis, se caracterizan por tener un átomo de nitrógeno con tres enlaces unido al grupo carbonilo.
Las amidas más sencillas son derivados del amoníaco.
Se puede considerar como un derivado de un ácido carboxílico por sustitución de grupo oxidrilo (-OH) del ácido por un grupo –NH2, -NHR ó –NRRl llamado grupo amino.
En síntesis, se caracterizan por tener un átomo de nitrógeno con tres enlaces unido al grupo carbonilo.
Las amidas más sencillas son derivados del amoníaco.
Amidas:
Una amida es un compuesto orgánico cuyo grupo funcional es del tipo RCONR'R'', siendo CO un carbonilo, N un átomo de nitrógeno, y R, R' y R'' radicales orgánicos o átomos de hidrógeno:
Se puede considerar como un derivado de un ácido carboxílico por sustitución del grupo —OH del ácido por un grupo —NH2, —NHR o —NRR' (llamado grupo amino).
Formalmente también se pueden considerar derivados del amoníaco, de una amina primaria o de una amina secundaria por sustitución de un hidrógeno por un radical ácido, dando lugar a una amida primaria, secundaria o terciaria, respectivamente.Concretamente se pueden sintetizar a partir de un ácido carboxílico y una amina:
Se puede considerar como un derivado de un ácido carboxílico por sustitución del grupo —OH del ácido por un grupo —NH2, —NHR o —NRR' (llamado grupo amino).
Formalmente también se pueden considerar derivados del amoníaco, de una amina primaria o de una amina secundaria por sustitución de un hidrógeno por un radical ácido, dando lugar a una amida primaria, secundaria o terciaria, respectivamente.Concretamente se pueden sintetizar a partir de un ácido carboxílico y una amina:































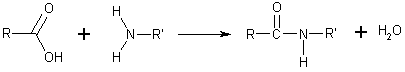
Sharon.Saludos.Queda registrado.Buen trabajo.
ResponderEliminarProf. Agustín